Cadastre-se e receba grátis as principais notícias do Correio.
Mounjaro: medicamentos podem ser importados com comprovação de uso pessoal
Caneta emagrecedora foi aprovada no país, mas ainda não está disponível nas farmácias
-
Thais Borges
Publicado em 1 de junho de 2024 às 05:00
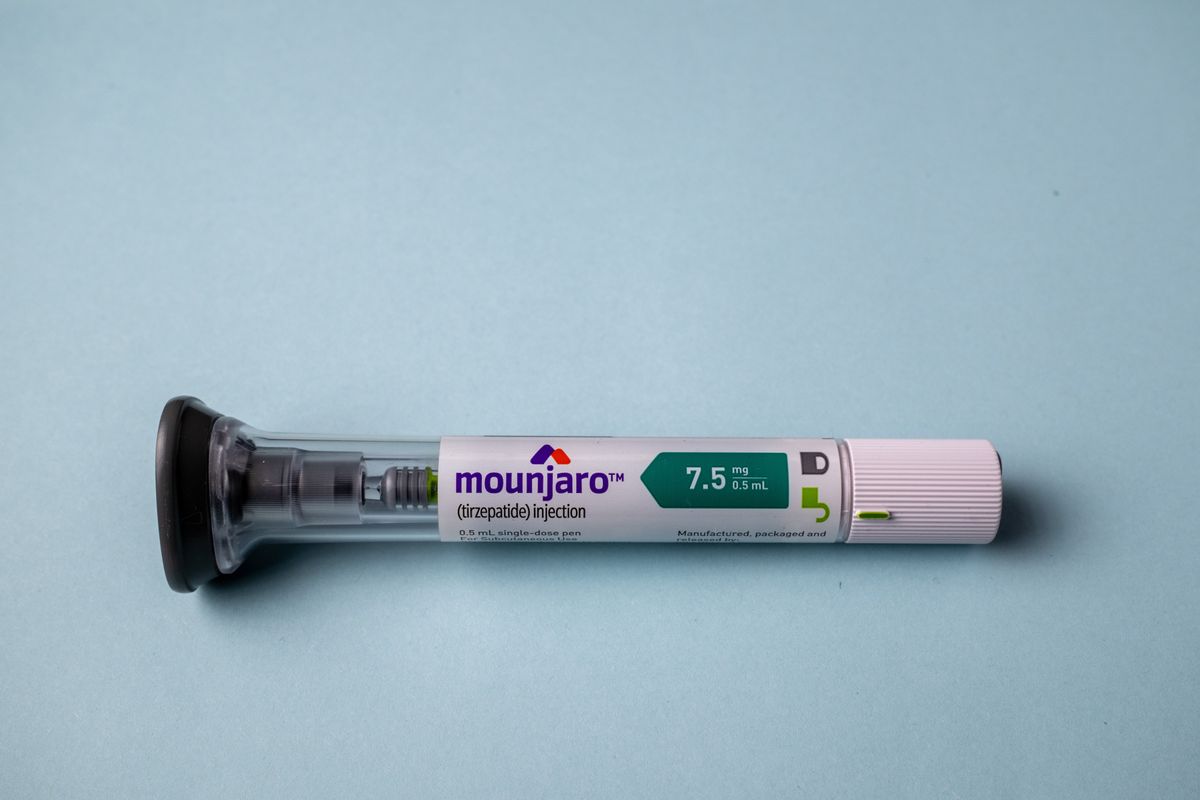
Uma pessoa em tratamento de saúde pode importar um medicamento no país, desde que apresente documentos que comprovem que é para uso próprio. Segundo o advogado René Viana, especialista em direito médico, é preciso observar se algum dos componentes do medicamento compõem a lista de substâncias sujeitas ao Controle Especial da Anvisa.
"Somente os medicamentos cujas substâncias estejam presentes na lista C1 da referida resolução poderão ser importados, quando não houver medicamentos semelhantes disponíveis no Brasil", diz ele, que é presidente da Comissão de Direito Médico e da Saúde da Ordem dos Advogados do Brasil - Seccional Bahia (OAB-BA). Alguns exemplos da lista são antidepressivos como o citalopram e anestésicos como o propofol.
No caso do Mounjaro, o advogado explica que o fato de o medicamento ter sido aprovado pela Anvisa implica dizer que ele passou por uma avaliação criteriosa de qualidade, segurança e eficácia. "No entanto, por não se tratar de uma medicação fabricada no Brasil, ainda persistem algumas etapas referentes ao processo de importação que precisam ser cumpridas pela empresa detentora do registro para que o medicamento, de fato, esteja disponível para compra no Brasil".
Ainda que a tirzepatida tenha sido aprovada para uso de diabetes tipo 2 no país, não significa que não é possível importá-la para pacientes com quadros de obesidade. Segundo Viana, em geral, a interpretação das autoridades sanitárias quanto ao uso 'off label' (ou seja, que não segue a bula) costuma ser restritiva. Assim, a importação pessoal com um objetivo diferente do que foi aprovado pode ter restrições.
"Todavia, esse obstáculo pode ser contornado por via judicial, a partir da interpretação de julgados do Superior Tribunal de Justiça que reconhecem a validade da prescrição médica para uso off label, quando o medicamento já se encontra aprovado pela Anvisa".
De acordo com o órgão federal, os documentos que devem ser apresentados incluem a declaração de uso com a responsabilização do paciente pelo transporte e acondicionamento do material; o relatório médico e a prescrição emitida por profissional de saúde habilitado com a quantidade a ser importada.
Através da assessoria, contudo, a Anvisa destacou que medicamentos comprados no exterior, por pessoa física, são considerados não regularizados. Assim, eles não tiveram a segurança e a eficácia avaliadas pela agência, podendo causar reações adversas inesperadas. O uso, portanto, é de responsabilidade do usuário e do profissional prescritor.
"Orientamos que o usuário busque, inicialmente, medicamentos devidamente registrados junto à Anvisa, cuja segurança e qualidade foi avaliada, e para os quais o detentor da regularização no país possui a responsabilidade por sua comercialização e disponibilidade ao consumo", acrescentam.





