Cadastre-se e receba grátis as principais notícias do Correio.
Sputnik e Covaxin: conheça as novas vacinas a serem aplicadas no Brasil
Na última sexta (4), a Anvisa aprovou a importação e uso restrito das duas vacinas; ainda não há previsão para a chegada dos imunizantes no país
-
Carolina Cerqueira
Publicado em 7 de junho de 2021 às 05:00
- Atualizado há 2 anos
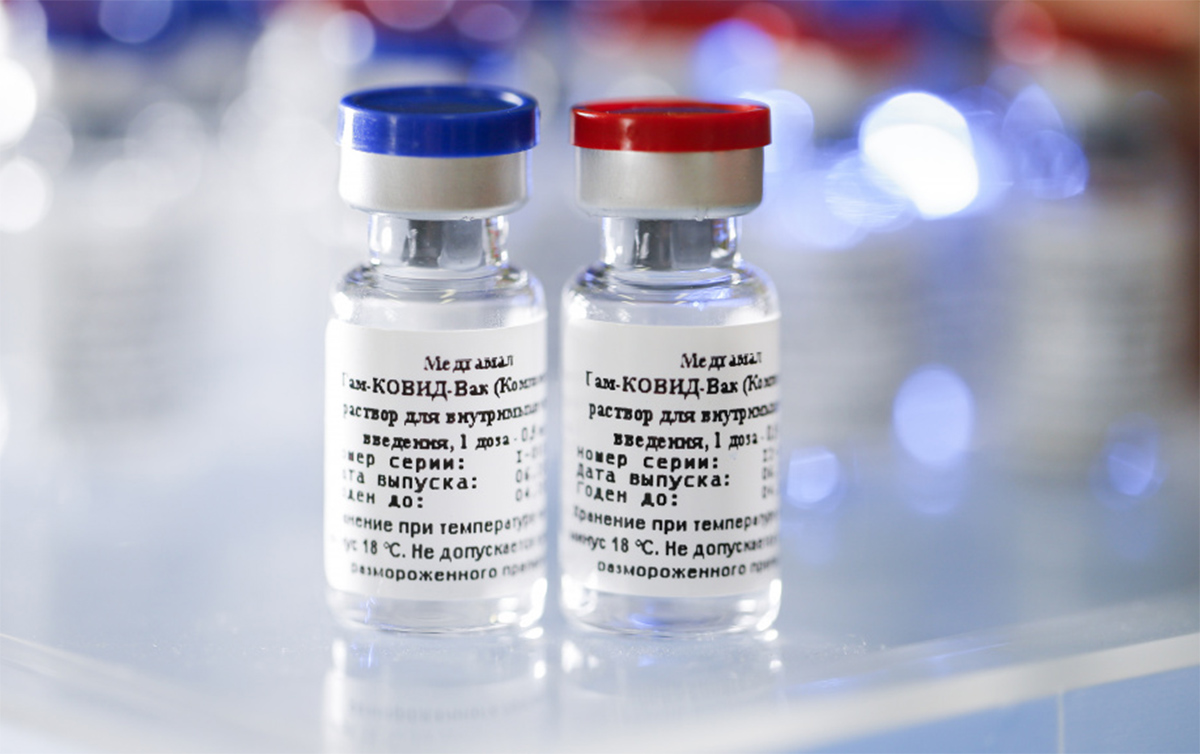
As primeiras doses da vacina russa Sputnik V devem chegar ao Brasil em julho. A informação foi dada à CNN pelo governador do Maranhão, Flávio Dino. Já de acordo com o secretário de saúde da Bahia, Fábio Vilas-Boas, ainda não é possível afirmar uma data. No sábado (5), gestores-chefes do Executivo das regiões Norte e Nordeste se reuniram para definir os próximos passos após a Agência Nacional de Vigilância Sanitária (Anvisa) autorizar a importação, sob condições controladas, de 928 mil doses da Sputnik V. Também foi aprovada a importação, nas mesmas medidas, de 4 milhões de doses da vacina indiana Covaxin, que ainda não têm previsão de chegada ao Brasil.
A aprovação da Anvisa, na última sexta-feira (4), faz com que a Sputnik V e a Covaxin se juntem à Coronavac, Astrazeneca/Oxford e Pfizer, todas já em uso no Brasil. Os dois novos imunizantes a entrarem na lista foram lançados antes mesmo da conclusão dos estudos, se tornando alvo de incertezas. Agora que chegam ao Brasil, serão aplicados com diversas restrições e exigências de acompanhamento. Entenda o porquê e o que se sabe sobre as duas vacinas:
Sputnik V Com a decisão da Anvisa, o Brasil se tornou o 67º país do mundo a autorizar a Sputnik V. Mas a marca poderia ter sido alcançada bem mais cedo. É que, ainda em março deste ano, o governo da Bahia anunciou um contrato para a compra de 9,7 milhões de doses da Sputnik V, como parte de negociação do Consórcio Nordeste com o Fundo de Investimentos Diretos da Rússia, que fornecerá 37 milhões de doses ao Brasil. A primeira remessa, que tinha previsão de chegar em abril, seria de 2 milhões de doses. Sem autorização da Anvisa, contudo, não houve remessas.
Agora, a Anvisa autorizou a importação por seis estados, no quantitativo equivalente a 1% da população de cada um. O estado da Bahia foi autorizado a importar 300 mil doses; o Maranhão, 141 mil doses; Sergipe, 46 mil doses; o Ceará, 183 mil doses; Pernambuco, 192 mil doses, e o Piauí, 66 mil doses. A agência informou que “vai analisar os dados de monitoramento do uso da vacina para poder avaliar os próximos quantitativos a serem importados”.
O secretário Vilas-Boas, em entrevista no sábado (5) à TV Bahia, informou que ações já estão sendo feitas para agilizar a chegada das doses da Sputnik à Bahia. “Estamos analisando de que forma podemos agilizar todas as condicionantes [impostas pela Anvisa]. Já dividimos elas. Uma pequena parte deverá ser providenciada pelo fundo russo e outra parte caberá a nós secretários estaduais de saúde, mas tudo dentro do previsto e do que já imaginávamos que seriam nossas responsabilidades de fazer todo o processo de acompanhamento de farmacovigilância da introdução dessa vacina no país”, afirmou o secretário.
Vilas-Boas, contudo, explicou que ainda não é possível dizer quando a vacina chegará em solo baiano. “Depende agora de uma conversa com os russos. Temos que fazer um ajuste legal no nosso contrato. O contrato que temos prevê uma quantidade de 37 milhões [de doses para o Nordeste] e nós vamos ter que fazer um aditivo informando que será de 1% inicialmente e, posteriormente, com a autorização definitiva da Anvisa, a gente poderá executar o resto do contrato”, destacou.
A Sputnik V foi o primeiro imunizante registrado contra a covid-19 no mundo. A vacina foi lançada pela Rússia em agosto de 2020, com testes ainda em andamento. A principal preocupação em torno do imunizante diz respeito ao tipo de tecnologia utilizada: vetor viral não replicante.
Isso significa dizer que os cientistas utilizaram adenovírus para simular no organismo a presença de uma ameaça mais perigosa e que se deseja combater para gerar uma resposta imune. Eles foram modificados para não serem capazes de se replicar depois que entram nas células humanas.
Ao contrário de outros imunizantes que também usam adenovírus, como o da AstraZeneca/Oxford e o da Janssen, a Sputnik V é a única a usar dois vetores: o Ad26 e o Ad5, um em cada dose. Esse é justamente o trunfo da vacina russa, em comparação com as outras.
"A ideia de modificar dois adenovírus diferentes é para reduzir uma possível resposta imune contra o próprio vetor. Por isso, ela tem uma eficácia maior do que as outras vacinas com vetor viral. A eficácia dela no estudo publicado foi acima de 90, enquanto as outras ficam em torno de 70% a 75%", diz a infectologista e imunologista Fernanda Grassi, pesquisadora da Fiocruz e integrante da Rede Covida.
Usar um adenovírus geneticamente modificado para que não se repliquem é algo relativamente comum - acontece em vacinas como a do ebola, por exemplo. Esse tipo de imunizante costuma ser considerado seguro pela comunidade científica.
O problema, segundo a Anvisa, é que os adenovírus usados nessa vacina poderiam, sim, se replicar e isso pode fazer mal à saúde de quem for imunizado com ela. O fato está ainda em discussão e documentos estão sendo solicitados para análise e conclusão.
“A Sputnik está sendo usada em mais de 60 países e não temos ouvido falar de efeitos ou reações graves. As reações que estão sendo observadas são normais de algumas vacinas. Quem recebe vacina pode ter febre, dor no local da aplicação, moleza, sintomas já esperados”, acrescenta Fernanda.
Covaxin Já a indiana Covaxin faz parte de um contrato do Ministério da Saúde com a Precisa Medicamentos/Bharat Biotec para compra de 20 milhões de doses. A previsão era da chegada de 8 milhões de doses ainda em março, mas a importação não foi autorizada. A decisão de sábado da agência regulatória brasileira permitiu, por enquanto, o uso de 4 milhões de unidades do imunizante.
A Anvisa ponderou o fato de não ter recebido relatórios da agência indiana, o curto prazo de acompanhamento dos participantes dos estudos e a inconclusão dos estudos da fase 3, etapa que atesta a eficácia da vacina.
A Covaxin usa versões inativadas do Sars-CoV-2. Essa é uma tecnologia tradicional e semelhante à utilizada pela Coronavac, do Instituto Butantan. “A partir do vírus inteiro, as substâncias químicas são inativadas e são adicionadas então substâncias que fazem aumentar a resposta imune”, explica a imunologista. A vacina, portanto, contém vírus mortos, incapazes de infectar pessoas, mas ainda capazes de instruir o sistema imunológico a montar uma reação defensiva contra uma infecção.
Vacinas com vírus inativados, como a Covaxin, têm tecnologia semelhante a de vacinas da gripe, poliomielite, entre outras. É uma plataforma bem estabelecida e considerada segura na produção de vacinas. “São as vacinas, digamos, mais fáceis de serem feitas. A vantagem é a facilidade e o fato de já conhecermos. Mas elas dão uma imunidade um pouco menor do que outras vacinas com outras tecnologias. Cada uma tem suas vantagens e desvantagens”, pontuou Fernanda.
Outra possível vantagem das vacinas com vírus inativados é o melhor funcionamento contra mutações. Parte dos imunizantes disponíveis hoje (como o da Pfizer e o da Astrazeneca) focam na proteína S, a spike, do agente infeccioso. Se esse trecho do vírus sofre mutações, é possível que as doses percam parte da eficácia, embora isso precise ser estudado. O produto da Barat Biotech, por outro lado, apresenta o vírus todo (inativado) ao sistema imune. Com isso, a chance de reconhecer o Sars-CoV-2 mesmo se ele sofrer alterações relevantes seria maior.
Aprovação com restrição A Anvisa considera que ainda faltam informações sobre os dois imunizantes - motivo pelo qual o pedido inicial foi negado em março, no caso da indiana Covaxin, e em abril, para a russa Sputnik V. Entretanto, por votação de 4 a 1, a diretoria colegiada decidiu que o atual momento da pandemia no Brasil justificaria aprovar a importação "com condicionantes". Isso significa que a Anvisa não se responsabiliza pela eficácia e segurança, mas permite a importação e aplicação restrita, entregando a responsabilidade aos fabricantes e compradores.
Caso o uso emergencial, que está, separadamente, em análise, seja reprovado pelo órgão brasileiro ou pela Organização Mundial da Saúde (OMS), os estados devem suspender a importação, distribuição e uso dos imunizantes imediatamente. A autorização do uso emergencial é dada pela Anvisa após a análise e constatação de eficácia e segurança de uma vacina.
Como ressaltou o gerente geral de medicamentos da Anvisa, Gustavo Mendes, nenhuma das duas vacinas deve ser usada por quem tem hipersensibilidade a qualquer dos componentes da fórmula, como grávidas, lactantes, menores de 18 anos, maiores de 60 anos, mulheres em idade fértil que desejam engravidar nos próximos 12 meses, pessoas que tenham enfermidades graves ou não controladas (cardiovascular, respiratória, gastrointestinal, neurológica, insuficiência hepática, insuficiência renal, patologias endócrinas) e antecedentes de anafilaxia.
Não poderão usá-las pessoas que tenham recebido outra vacina contra a covid-19, apresentem febre, tenham HIV e hepatite B ou C, tenham se vacinado nas quatro semanas anteriores, tenham recebido imunoglobulinas ou hemoderivados três meses antes, tenham recebido tratamentos com imunossupressores, citotóxicos, quimioterapia ou radiação nos últimos 36 meses e que tenham recebido terapias com biológicos incluindo anticorpos anticitocinas e outros anticorpos.
As 5 vacinas aprovadas no Brasil: (quadro comparativo)
*No Brasil, nenhuma vacina está sendo aplicada em pessoas com menos de 18 anos.
Sputnik VFabricante: Instituto Gamaleya de Pesquisa (Rússia). Tipo de tecnologia: Vetor viral não replicante. Data de aprovação pela Anvisa: 4 de junho de 2021. Tipo de aprovação: Importação de lotes com restrições Quantidade de doses: Duas. A aplicação precisará ter atenção redobrada, pois o conteúdo da primeira e da segunda dose da Sputnik são diferentes. Intervalo entre as doses: 21 dias (com possibilidade de ser ampliado para três meses) Taxa de eficácia: 91%. Efeitos colaterais: Comum - doença semelhante à gripe, dor de cabeça, fadiga, reações no local da injeção. Foi confirmado pelo Comitê Independente de Monitoramento de Dados que nenhum evento adverso sério relacionado à vacina foi observado. Covaxin Fabricante: Bharat BioTech (Índia). Tipo de tecnologia: Vírus inativado. Data de aprovação pela Anvisa: 4 de junho de 2021 Tipo de aprovação: Importação de lotes com restrições. Quantidade de doses: Duas. Intervalo entre as doses: 4 semanas. Taxa de eficácia: 78% (100% em casos graves) Efeitos colaterais: Estudos publicados sobre as fases 1 e 2 não mostram efeitos colaterais graves. CoronavacFabricantes: Sinovac (China) e Instituto Butantan (Brasil). Tipo de tecnologia: Vírus inativado. O coronavírus é inativado por ação do calor ou de algum produto químico. Quando o corpo recebe a vacina, o vírus inativado faz com que o corpo gere anticorpos contra a covid-19. Isso porque as células de resposta imune “capturam” o vírus inativado e ativam a ação dos chamados linfócitos, células que são especializadas em combater microrganismos. São elas que produzem os anticorpos, que impedem que o vírus infeste outras células e fiquemos doentes. Data de aprovação pela Anvisa: 17 de janeiro de 2021. Tipo de aprovação: Emergencial. Quantidade de doses necessárias: Duas. Intervalo entre as doses:2 a 4 semanas. Taxa de eficácia: 50% (Pode chegar a 62%) Efeitos adversos: Muito comum - dor no local da aplicação, dor de cabeça, cansaço. Comum - cansaço, febre, dor no corpo, diarreia, náusea, dor de cabeça, enjoo, dor muscular, calafrios, tosse, perda de apetite, coceira, coriza. Incomum - vômitos, dor abdominal inferior, distensão abdominal, tonturas, tosse, perda de apetite, reação alérgica, pressão arterial elevada, hipersensibilidade alérgica ou imediata, inchaço, coceira, vermelhidão, diminuição da sensibilidade, endurecimento, hematoma, vertigem Astrazeneca/OxfordFabricantes: AstraZeneca (Inglaterra/Suécia), Universidade de Oxford (Inglaterra) e Fundação Oswaldo Cruz (Brasil). Tipo de tecnologia: Vetor viral não replicante. A vacina produzida pela Universidade de Oxford (Reino Unido) usa um "vírus vivo", como um adenovírus que provoca um resfriado comum, modificado para conter instruções para a produção de uma proteína característica do coronavírus. No entanto, na proporção aplicada, ele não tem capacidade de se replicar e prejudicar a saúde humana. Quando rompe as células, esse adenovírus estimula a produção dessa proteína, que é detectada pelo sistema imune. A partir daí, o corpo cria uma resposta contra o coronavírus. Data de aprovação pela Anvisa: 17 de janeiro de 2021. (Uso emergencial) Tipo de aprovação: Definitiva. (12 de março de 2021) Quantidade de doses: Duas. Intervalo entre as doses: 12 semanas. Taxa de eficácia (global possível): 81%. Observação: No Brasil, não está sendo aplicada em gestantes. Efeitos adversos: Muito comum - sensibilidade, dor, sensação de calor, coceira ou hematoma, indisposição, cansaço, calafrio, febre, dor de cabeça, enjoo, dor muscular ou nas articulações. Ocorrem em 1 em cada 10 pessoas. Comum - inchaço, vermelhidão ou um caroço no local da injeção, febre, enjoos, diarreia, sintomas semelhantes a resfriado, dor de garganta, coriza, tosse. Ocorrem em 1 em cada 10 pessoas. Incomum - sonolência, tontura, diminuição do apetite, dor abdominal, ínguas, suor, coceira ou erupção na pele. Ocorrem em 1 em cada 100 pessoas. Muito raro - coágulos sanguíneos graves em pessoas com níveis baixos de plaquetas. Foram observados com uma frequência inferior a 1 em 100.000 indivíduos vacinados. Desconhecido - reação alérgica grave, inchaços graves nos lábios, face, boca e garganta. Não pode ser calculada a partir dos dados disponíveis PfizerFabricantes: Pfizer (Estados Unidos) e BioNTech (Alemanha). Tipo de tecnologia: mRNA. A vacina é criada a partir da replicação de sequências de RNA que mimetizam a proteína spike, específica do vírus Sars-CoV-2. Essa versão consegue desencadear uma reação do sistema imunológico, que cria uma defesa, sem causar danos à saúde. Data de aprovação pela Anvisa: 23 de fevereiro de 2021. Tipo de aprovação: Definitiva. Quantidade de doses: Duas. Intervalo entre as doses: 12 semanas. Taxa de eficácia (global possível): 95%. Efeitos adversos: Muito comuns - dor e inchaço no local da injeção, cansaço, dor de cabeça, diarréia, dor muscular, dor nas articulações, calafrios e febre. Ocorrem em 10% dos pacientes. Comuns - vermelhidão no local de injeção, náusea e vômito. Ocorre entre 1% a 10% dos pacientes. Incomuns - aumento dos gânglios linfáticos, reações de hipersensibilidade [lesão na pele ou coceira, inchaço da pele ou mucosa, sensação de mal estar, dor no braço, insônia e prurido no local de injeção. Ocorrem entre 0,1% e 1%.. Rara - paralisa facial aguda. Ocorrem entre 0,01% e 0,1%. Desconhecido - reação alérgica grave (anafilaxia).
*Com orientação do chefe de reportagem Jorge Gauthier








